수정 전해탈지
^ Electolytic Degreasing
수용액을 전해하여 발생되는 가스 (음극(H2) 또는 양극 (O2) 에 발생하는 가스) 에 의하여 소재 표면에 부착된 이물질과 유지분을 이탈시켜 탈지용액 속에 분산 또는 검화하여 제거하는 방법으로 양극전해탈지, 음극전해탈지, 전해탈지 등이 있으며 경우에 따라 전처리로 예비탈지가 필요할 수 있다.
일반적으로 올소규산소다를 이용하지만 양극전해탈지를 하면 무수규산이 유리되어 소재표면에 피막을 형성하므로 양극탈지에는 적합치 않다. 비이온 계면활성제를 혼합 사용한다.
4OH- → 2H2O + O2+ 4e- : 산소 (O2) 발생
양극을 이용한 탈지로서 산화 반응 4(OH)– = 2H2O + O2(g) + 4e- 를 촉진하기 위해 수용액에서 사용된다. 산소 가스는 오염된 소재표면에 직접 작용하여 녹, 부착물 및 오일 등과 같은 오염물질을 제거한다.
4H2O + 4e- → 4OH +2H2 : 수소 (2H2) 발생
음극으로 이용한 탈지 방법으로 소재표면에서는 환원 반응이 생기기도 한다. 수용액의 pH 는 반응을 유지하기 위해 충분한 수소 이온을 공급하여야 한다. 4H+ + 4e- = 2H2(g) 와 같은 방식으로 금속 표면에서 녹이나 산화물과 같은 오염물질을 제거하게 된다.
70 kg 올소규산소다
25 kg 메타규산소다
25 kg 삼인산소다
25 kg 탄산소다
1 kg 비이온 계면활성제
3 kg 음이온 계면활성제
- 사용량 50 g/ℓ, (-)/(+) 전해, 60 ℃
수정 참고
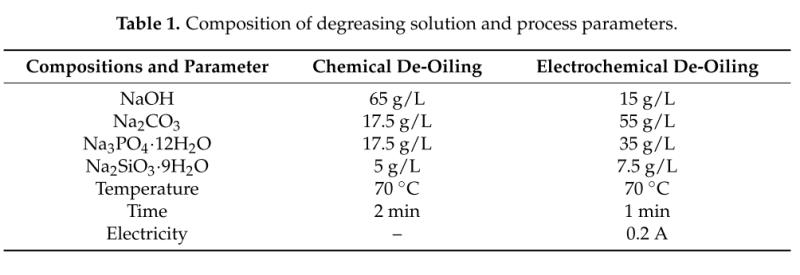
"~ the Current Density of the Electrolyte on the Texture and Mechanical Properties ~"




